BioMarin社は、BioMarin R&D DAY 2018にて以下の発表を行いました。フェーズ2・3の最新情報に加え、無投与状態での患者との最終身長の比較研究について情報開示がなされています。
—————————
Vosoritide Data Update
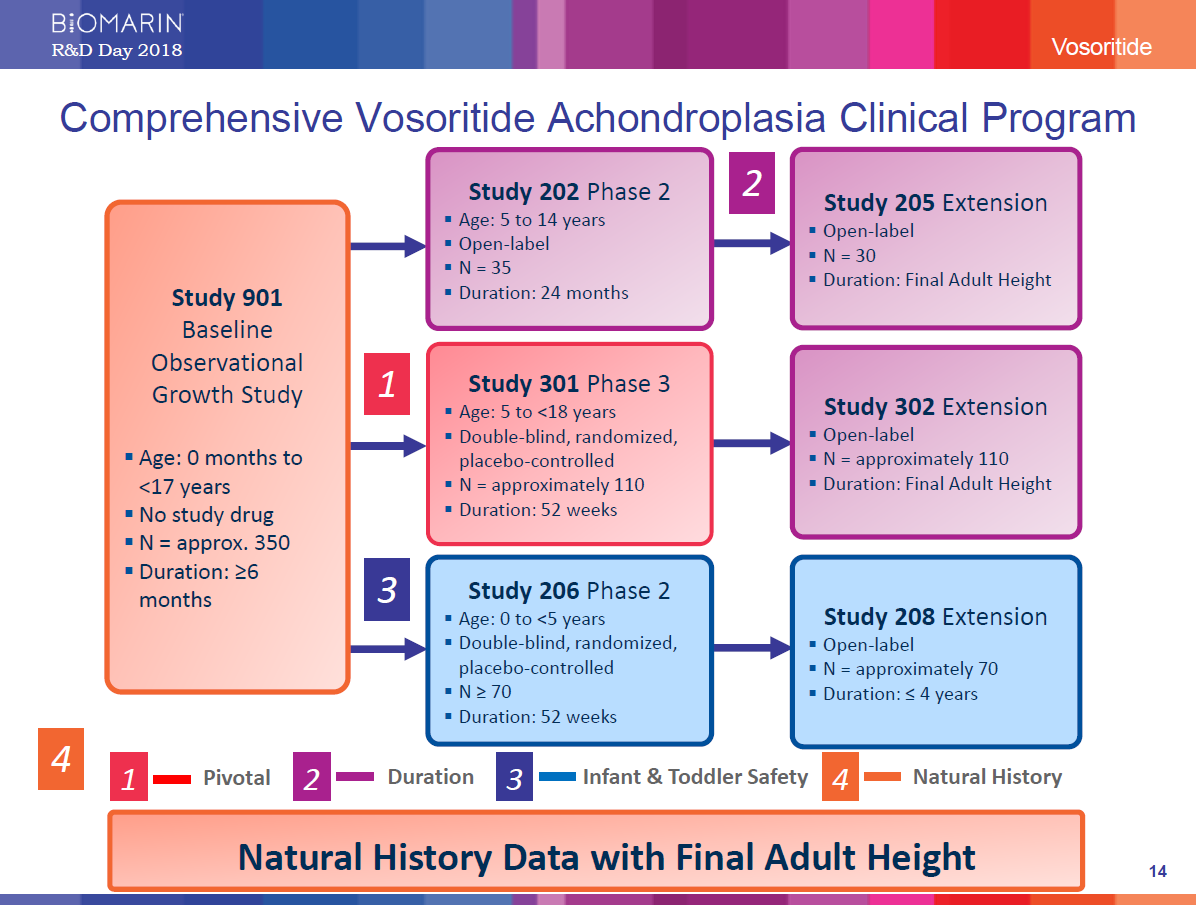
BioMarin provided an update on its clinical program for vosoritide, an analog of C-type Natriuretic Peptide (CNP), in children with achondroplasia, the most common form of disproportionate short stature in humans.
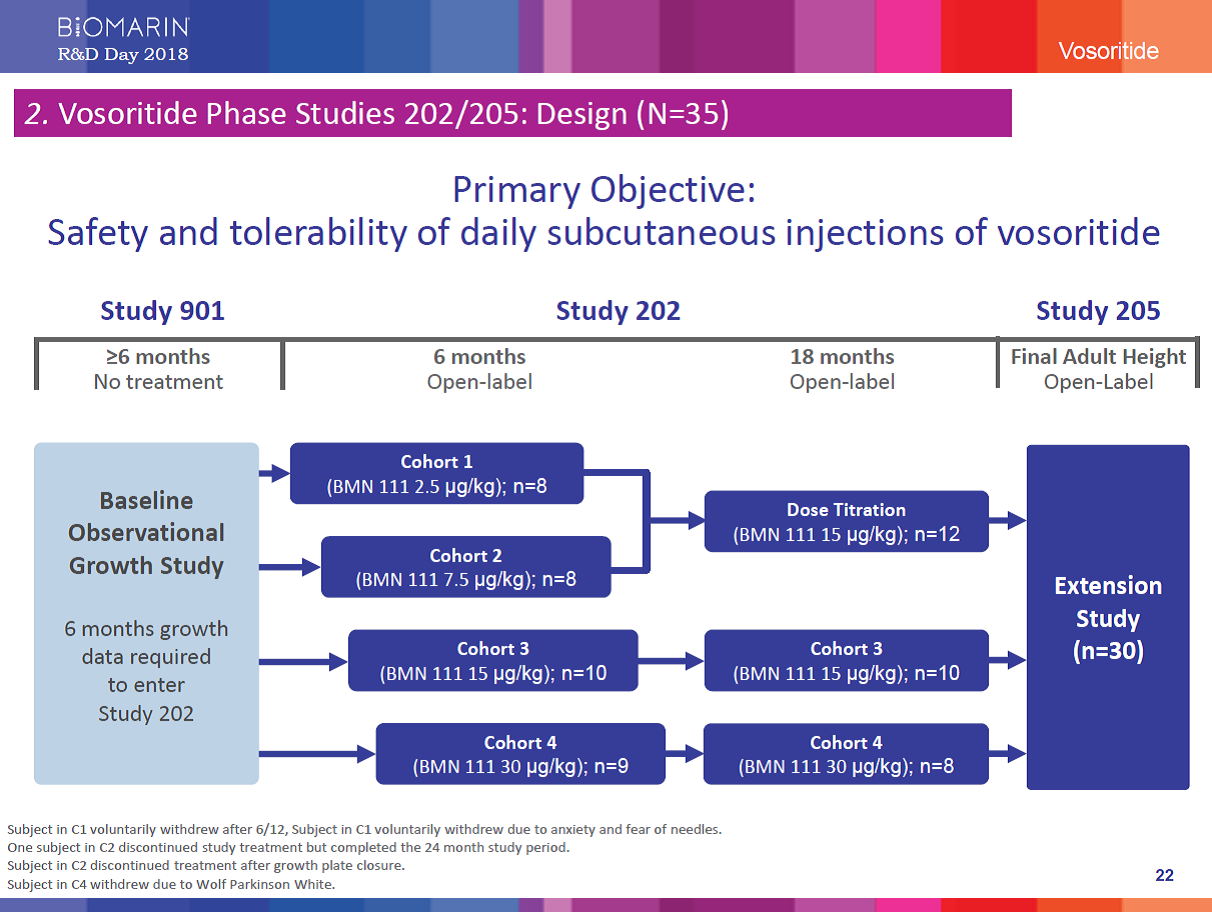
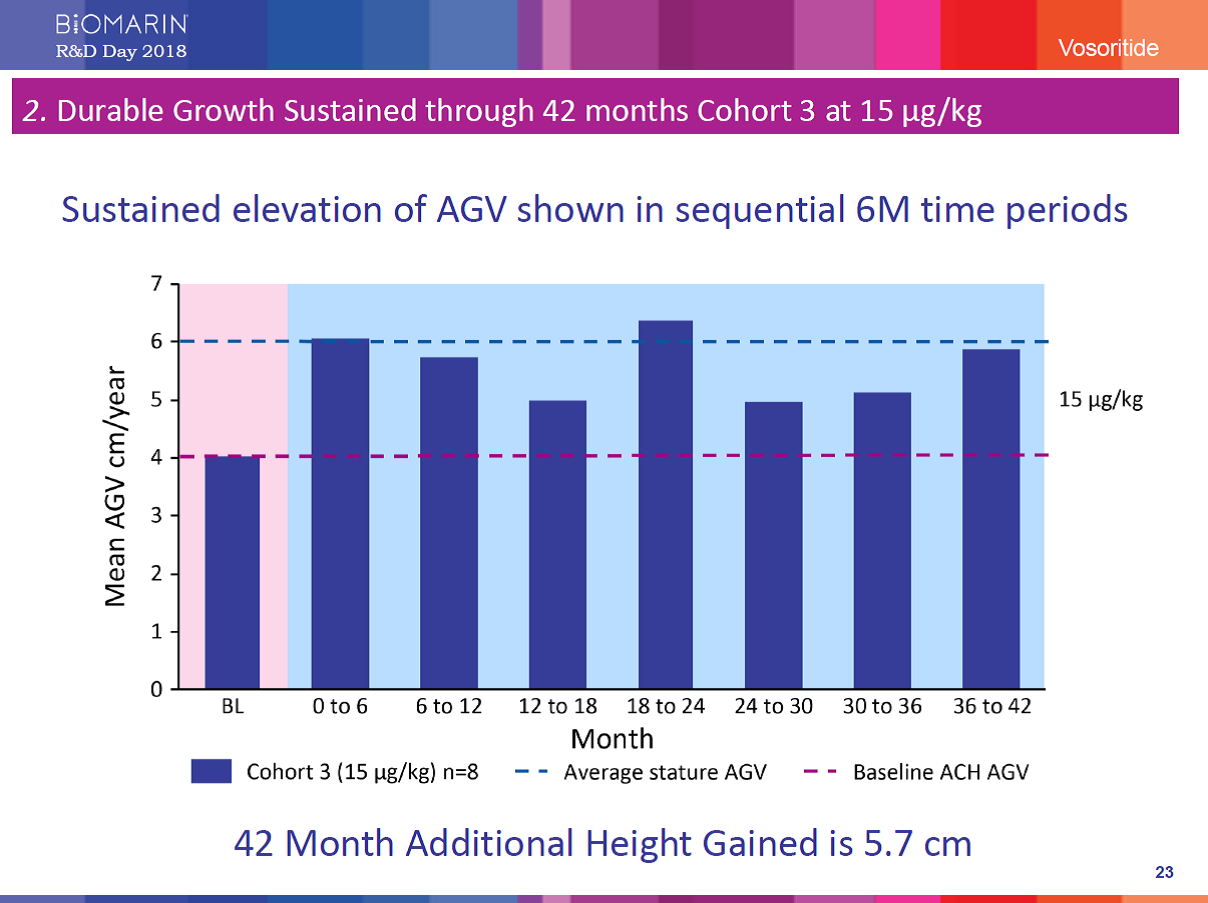
An ongoing open-label, Phase 2 study of vosoritide for achondroplasia demonstrated sustained increase in cumulative height gained over 42 months of treatment in children in cohort 3 at a dose of 15 µg/kg/day. The cohort gained a mean of 5.7 cm of cumulative height over what the participants’ baseline would have predicted. At 30 months, the same cohort experienced a 4 cm increase over what the participants’ baseline growth velocity would have predicted.
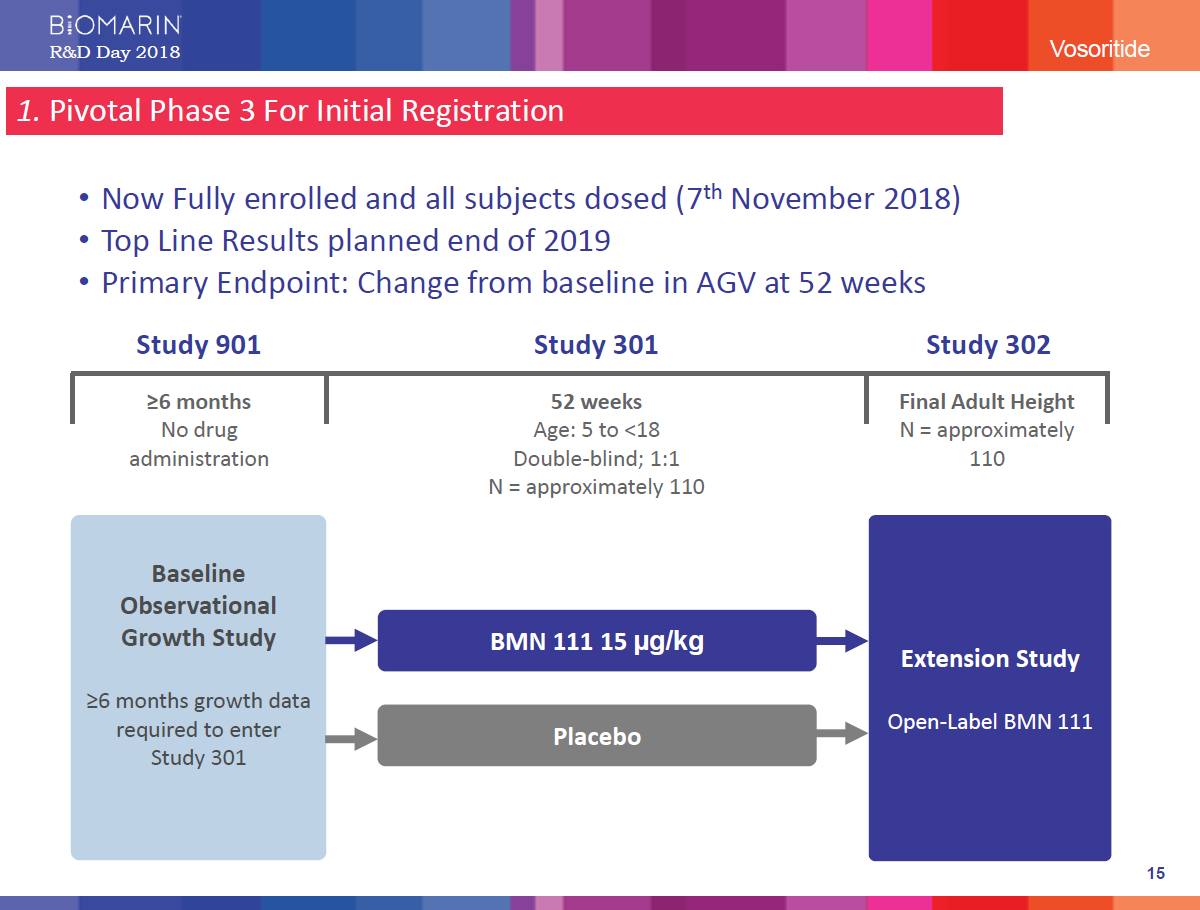
BioMarin announced today that the Phase 3 study of vosoritide in children is now fully enrolled and top line results are planned for the end of 2019. BioMarin has also initiated a global Phase 2 study in infants and young children up to age 5 with achondroplasia.
In addition to clinical studies of vosoritide, in collaboration with the leading skeletal dysplasia centers in the United States (U.S.), BioMarin is conducting a multi-center, natural history study in 1,377 people with achondroplasia. This natural history study will make it possible to compare the final adult height of people treated with vosoritide in our clinical studies and those not treated. These data will support the assessment of efficacy of vosoritide.
Vosoritide has been granted orphan drug designation in both the U.S. and Europe.
Source: BioMarin Press release” BioMarin Highlights Breadth of Innovative Development Pipeline at R&D Day on November 7th in New York”
—————————
Vosoritide データ・アップデート
BioMarin社は、小児軟骨無形成症患者に投与中のVosoritide(C型ナトリウム・ペプチド(CNP)アナログ)の臨床試験において最新情報を発表しました。
オープンラベルで進行中のフェーズ2において、15μg/ kg /日の投与群(コーホート3)にて累積で42ヶ月間と治療期間を経て、被験者の成長速度はベースライン(4cm)を越え、平均5.7cm/年の成長速度を記録しました。同投与群は、30ヶ月目において、ベースラインより予測できる成長速度よりも4cmの増加が得られました。
今般、フェーズ3試験の被験者全員のエントリーが完了し、2019年末に最初の結果が得られるとの計画です。
また、5歳以下の乳幼児を対象としたグローバルフェーズ2試験も既に開始されています。
Vosoritideの臨床試験に加えて、アメリカの先進的な骨形系統疾患の医療機関と協力して、バイオマリンは、軟骨無形成症患者1,377人を対象とした複数施設におけるナチュラル・ヒストリー研究を実施しています。この研究は、Vosoritideで治療した患者とそうでない患者の最終的な成人の身長との比較が可能となります。当研究結果は、Vosoritideの有効性評価を補完するものとなります。
Vosoritideは、欧米でのオーファンドラッグ指定を受けています。
Source: GTA translation of BioMarin Press release” BioMarin Highlights Breadth of Innovative Development Pipeline at R&D Day on November 7th in New York”