2023 年3月6日(東部標準時(EST))、QED親会社であるBridgeBio Inc.は、小児の軟骨無形成症の開発中の治療薬Infigratinibについて、以下のプレスリリースを発表しました。本プレスリリースをGTAが日本語に翻訳し、配信するものです
※本資料の正式言語は英語であり、その内容、解釈および補足情報については正式言語が優先します。詳細はSourceをご参照ください。
――――――――――――――――――――――
BridgeBio、軟骨無形成症の治療薬“infigratinib”の第 2 相試験における5つのコホートの肯定的な結果を発表、治療に関連する有害事象はなく年率換算で 3.03 cm/年の成長速度の平均増加を示す
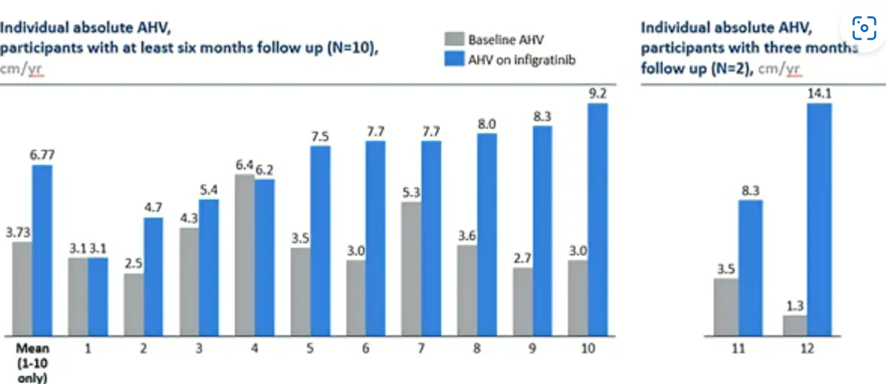
– 最高用量レベル(コホート5、1日1回0.25 mg / kg)つまり少なくとも6か月の追跡を受けた最初の10人の小児において、6か月の年間成長速度(AHV)のベースラインからの平均変化は+3.03 cm / yr(p = 0.0022)を示した。まだ6か月の追跡を受けていない残り2人の小児は、3か月のデータでAHVのベースラインからの平均変化が+ 8.8 cm /年を示した。
– ベースライン AHV からの少なくとも 25% の増加によって定義されるように、6 か月時点で小児の 80% が反応。当該小児の AHV のベースラインからの平均変化は 3.81 cm/年。
– 治療の結果、絶対 AHVの中央値は 7.6 cm/年に達し、これは軟骨無形成症の小児の成長の 99 パーセンタイルを超えた。
– infigratinibは、1 日 1 回の経口療法として明確な用量反応性を示し、コホート5で治療に関連すると評価された有害事象(AE)はなく、良好な忍容性を示した
– 良好なフェーズ 2 の結果に基づいて、BridgeBioは極めて重要な第3相試験への小児の登録を開始した
– BridgeBioは、軟骨無形成症と密接に関連し、線維芽細胞増殖因子受容体 3 (FGFR3) 機能獲得バリアントによって引き起こされる骨格異形成症である軟骨低形成症に対するinfigratinibの臨床開発を開始する予定であり、インフィグラチニブの今後の研究における軟骨無形成症の医学的および機能的合併症への影響を引き続き調査する。
――――――――――――――――――――――――――
2023 年3月6日、カリフォルニア州パロアルト発 (GLOBE NEWSWIRE) — 遺伝性疾患と癌に焦点を当てた商業段階のバイオ医薬品企業である BridgeBio Pharma, Inc. (Nasdaq: BBIO) (BridgeBio) は本日、PROPEL2 からの良好な結果を発表しました。軟骨無形成症の小児を対象とした治験薬 infigratinib の第 2 相試験であり、クラス最高の有効性と明確な安全性プロファイルの可能性を示しています。 infigratinibは、FGFR3 を阻害し、軟骨無形成症をその発生源で標的とするように設計された経口低分子です。 BridgeBioはまた、2023 年3月6日午前 7 時 30 分 (米国東部時間) に投資家向けの電話会議を開催し、第 2 相試験の結果についてお話します。
現在までの臨床試験の主な結果は次のとおりです。
- これまでに評価された最高用量レベル (コホート 5、0.25 mg/kg 1 日 1 回) では、6 か月間通院した 10 人の小児のベースラインからの年間身長速度 (AHV) の平均増加は +3.03 cm/年 ( p = 0.0022)。 個々のデータは、図 1 参照。
- 6 か月の通院を行った 10 人の小児のベースライン AHV は、軟骨無形成症の小児の予測範囲内で、3.73 cm/年であり、治療後は 6.77 cm/年に上昇。
- まだ 6 か月の追跡調査を受けていない残りの 2 人の小児は、3 か月で AHV のベースラインからの平均変化が +8.8 cm/年。 コホートの平均年齢は7.24歳。
- 6 か月間通院した 10 人の小児のうち 80% が反応し、ベースライン AHV からの変化は少なくとも 25%。該当被験者のAHV のベースラインからの平均変化は +3.81 cm/年。
- コラーゲン X (CXM) レベルの予備分析でも、コホート 5 でベースラインから統計的に有意な増加が見られた (p=.03)。 CXM は軟骨細胞主導の増殖のゴールド スタンダード バイオマーカーであり、infigratinibに対する強力な反応をさらに検証する。
- 以前に報告されたコホート 4 の AHV 値のベースラインからの変化 +1.52 cm/年と組み合わせると、コホート 5 のデータは、infigratinibの強い用量反応を示した。
- すべてのコホートの追跡期間の中央値は 71.1 週間です。 現時点で、この研究は忍容性の高い安全性プロファイルを示しており、コホート 5 では治験薬に関連する治療に関連する緊急有害事象 (TEAE) はなった。重篤な有害事象 (SAE) や AE による中止は、どのコホートでも報告されていいない。
PROPEL2の主任研究員で、臨床遺伝学者であり、オーストラリアのマードック小児研究所の分子療法研究のグループリーダーである Ravi Savarirayan 医学博士 (M.D.、Ph.D.) は、次のように述べています。「コホート 5 のデータは、軟骨無形成症の小児の年間身長速度に大きな影響を与え、これまでのところ優れた安全性プロファイルを示しています。 私たちは、これらの有望な結果を見て興奮しており、この規模のAHVの増加が、軟骨無形成症の医学的および機能的合併症の改善につながると考えています。第 3 相のピボタル臨床試験の開始に向けて次のステップを踏み出すことに歓喜しています」。
BridgeBio の創設者兼 CEO である Neil Kumar 博士は、次のように述べています。「私はこれらの有効性と安全性の結果に励まされており、この研究における医師、地域の擁護者、小児、および家族とのパートナーシップに感謝しています。これらの結果は有効性の新たな段階に到達し、当社の差別化された安全性と利便性プロファイルと相まって、軟骨形成不全症やその他の骨格異形成症の子どもたちにサービスを提供する機会を提供するでしょう。 私たちは、軟骨無形成症、軟骨低形成、およびその他の骨格異形成症の広範な医学的および機能的影響に対するinfigratinibの可能性を探求することを楽しみにしています」。
現在までの肯定的な結果に基づいて、BridgeBio は第3相試験の慣らし運転への小児の登録を開始しました。さらに、BridgeBioは、軟骨無形成症と密接に関連し、同様に FGFR3 機能獲得バリアントによって引き起こされる骨格異形成症である軟骨低形成におけるinfigratinibの臨床開発を開始する予定です。 BridgeBio は以前、ENDO 2022 および ASHG 2022 で軟骨低形成症の有望な前臨床データを発表しました。
The MAGIC Foundation のエグゼクティブ ディレクターである Dianne Kremidas 氏は、次のように述べています。「軟骨無形成症は、人全体に影響を与える幅広い影響を与える可能性があります。患者さんは、大後頭孔狭窄症、脊柱管狭窄症、心血管合併症、睡眠呼吸障害、肥満など、さまざまな医学的合併症を経験する可能性があり、時には外科的介入が必要になることもあります。潜在的な医学的および身体的合併症に加えて、軟骨無形成症の患者さんは、この状態で生活した結果、社会的および感情的な影響も経験する可能性があります。軟骨無形成症患者の全体的な健康、独立した機能、生活の質に影響を与える全身状態として、これに対処する可能性のある治療法を開発するというBridgeBio の使命に、私たちは感化されます」 。
Infigratinibは、少なくとも2041年まで知的財産保護を受けます。


